
Analisis Titrasi Pengertian, Prinsip Dasar, Jenis, Rumus, Syarat
Titik ekivalen adalah titik di mana jumlah mol zat dalam larutan titran sama dengan jumlah mol zat dalam larutan analit, sesuai dengan reaksi kimia yang berlangsung. Sedangkan titik akhir adalah titik di mana perubahan yang dapat diamati, seperti perubahan warna indikator, menandakan bahwa titrasi telah selesai. Jenis-Jenis Titrasi dan.

Titrasi Pengertian Jenis Dan Cara Melakukannya Ibs Riset
Seperti namanya, itu adalah titrasi dasar. Jumlah titran yang diketahui ditambahkan dari burret ke sampel titrat yang diambil dalam labu. Di sini satu zat dianalisis untuk kuantitasnya dengan zat lain dengan volume dan konsentrasi yang diketahui. 2. Titrasi Tidak langsung: Secara teoritis, mengubah zat menjadi asam dan menganalisis dengan basa.
An Advanced Guide to Titration Microlit
Titran (Titer) Titran adalah zat yang digunakan untuk mentitrasi. Titran disebut juga sebagai titer. Titran ini merupakan larutan standar yang telah diketahui secara pasti konsentrasinya, misalnya asam kuat atau basa kuat. Nah, pada titrasi asam basa, posisi titran terletak pada buret. b. Buret
:max_bytes(150000):strip_icc()/usa-education-metsa-students-in-class-539638000-58d521955f9b584683b8d1b0.jpg)
Apa itu Titran? Tinjau Konsep Kimia Anda
Contoh-contoh paling umum untuk proteksi titran ini adalah penyimpanan titran peka cahaya di dalam botol gelap, misalnya, larutan yodium, perlindungan titran Karl Fischer dari uap menggunakan, misalnya, ayakan molekular atau gel silika, dan perlindungan beberapa basa kuat tertentu, seperti sodium hidroksida, dari penyerapan karbon dioksida.

Jenis dan Metode Titrasi, Cara Melakukan yang Baik dan Benar, Praktikum
Salah satu senyawa kompleks yang biasa digunakan sebagai titran pada titrasi kompleksometri adalah Etilen Diamin Tetraacetic Acid (EDTA) Titrasi Karl Fischer. Seperti namanya, titrasi jenis ini menggunakan reagen Karl Fischer sebagai pereaksi, dimana reagen Karl Fischer terdiri atas SO 2 , I 2 , larutan basa, dan alkohol.

Konsep Dasar Analisis Titrimetri YouTube
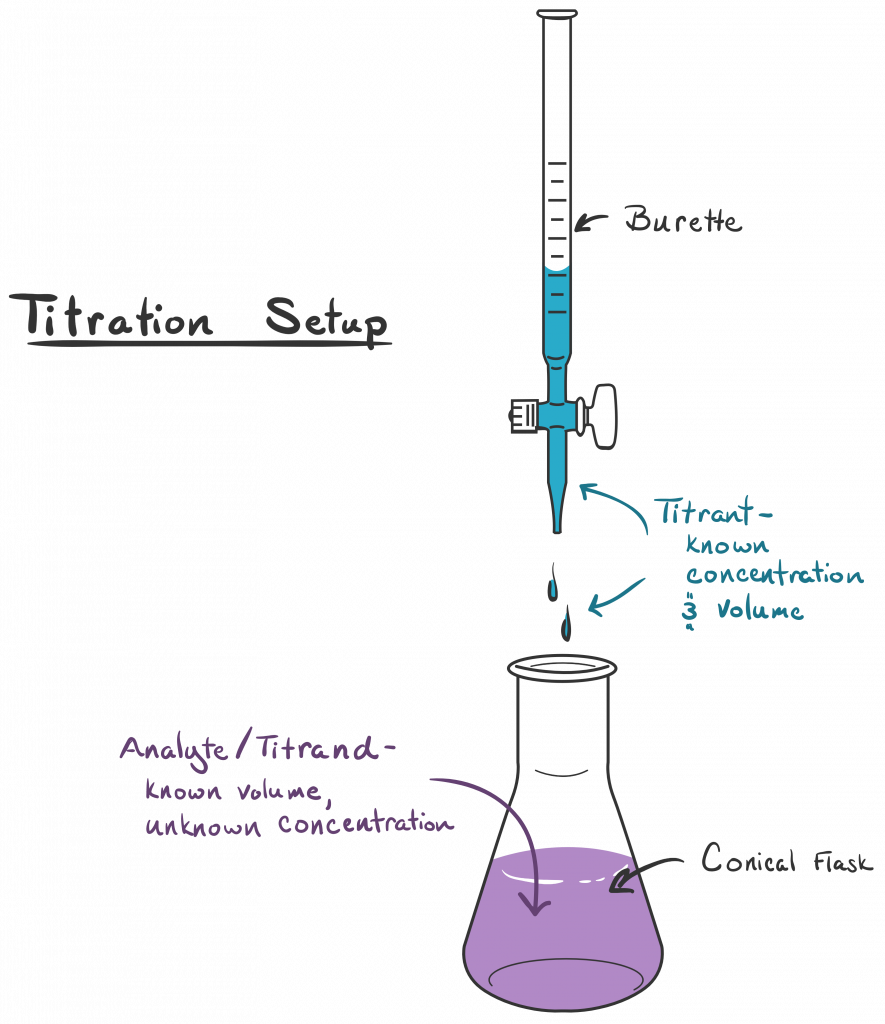
Pengertian Titrasi. Titrasi adalah metode laboratorium yang umum dalam analisis kimia kuantitatif untuk menentukan konsentrasi dari analit. Dalam ilustrasi dibawah ini, larutan dengan konsentrasi yang diketahui (disebut titran) digunakan untuk menentukan konsentrasi dari larutan yang tidak diketahui konsentrasinya (analit). Ilustrasi Titrasi.

Gambar di samping menunjukkan salah satu langkah d...
Titrasi adalah teknik analitik yang memungkinkan penentuan kuantitatif zat tertentu yang dilarutkan dalam sampel dengan penambahan reagen dengan konsentrasi yang diketahui. Teknik ini didasarkan pada reaksi kimia yang lengkap antara zat (analit) dan reagen (titran). Titran ditambahkan sampai reaksi selesai. Agar sesuai untuk penentuan, akhir.
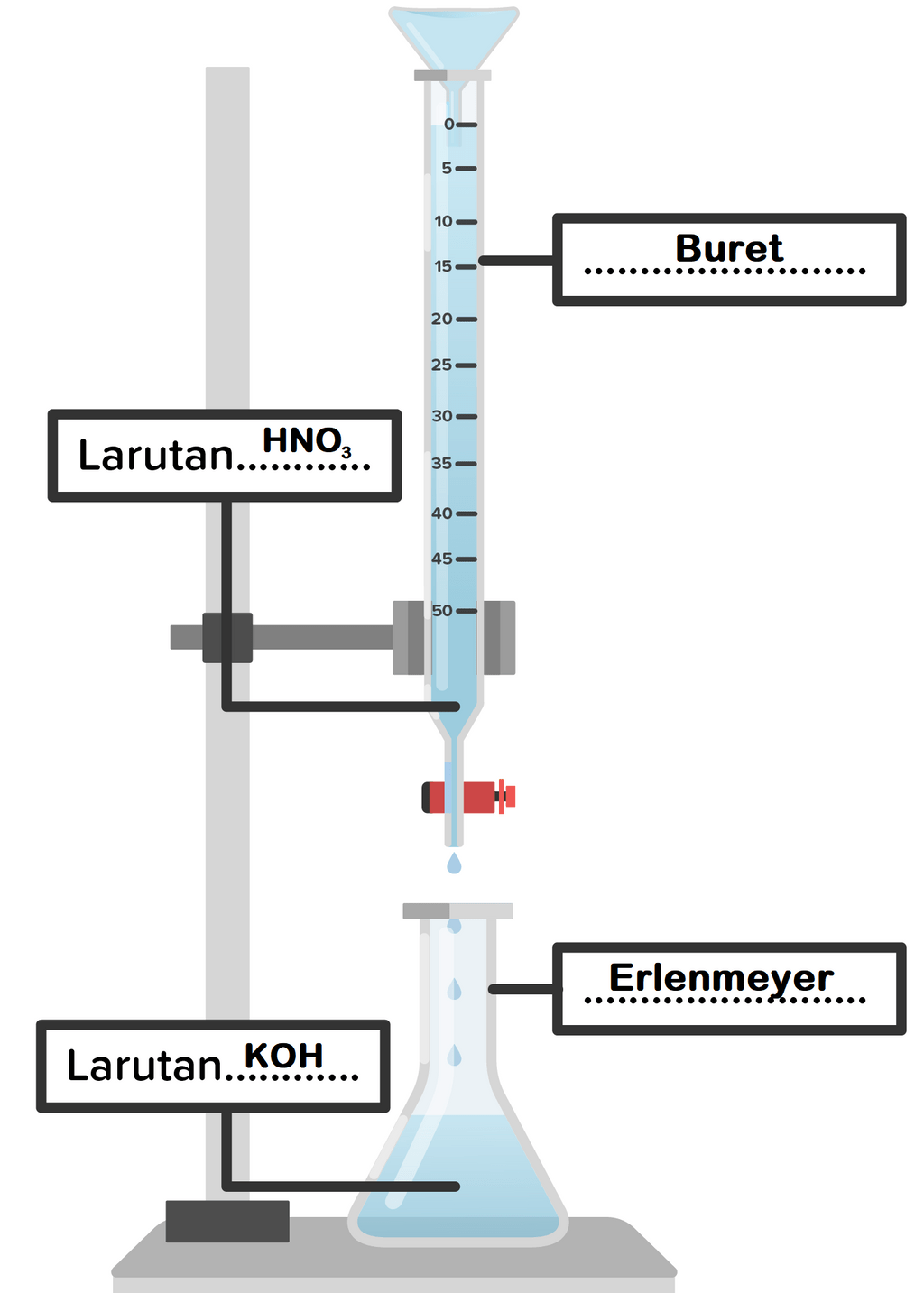
Seorang siswa akan melakukan praktikum titrasi asa...
Tujuan dilakukannya standarisasi adalah untuk mengetahui konsentrasi dari titran dan mencegah kesalahan pengujian dikarenakan titran yang rusak. Maka dari itu standarisasi sebaiknya dilakukan secara berkala sebelum titrasi sehingga hal itu akan mengantisipasi ketika terjadi kerusakan pada titran yang menyebabkan perubahan konsentrasi.

Titrasi Asam Basa Pengertian Prinsip Cara Tumus Jenis My XXX Hot Girl
Titran adalah larutan standar yang telah diketahui konsentrasinya. Indikator asam basa adalah zat yang mengalami perubahan warna ketika mendekati titik ekivalen. Misalnya, larutan yang akan dicari konsentrasinya (analit) adalah larutan asam berupa asam klorida (HCl). Prosedur titrasinya adalah: Memasukkan titran ke dalam buret
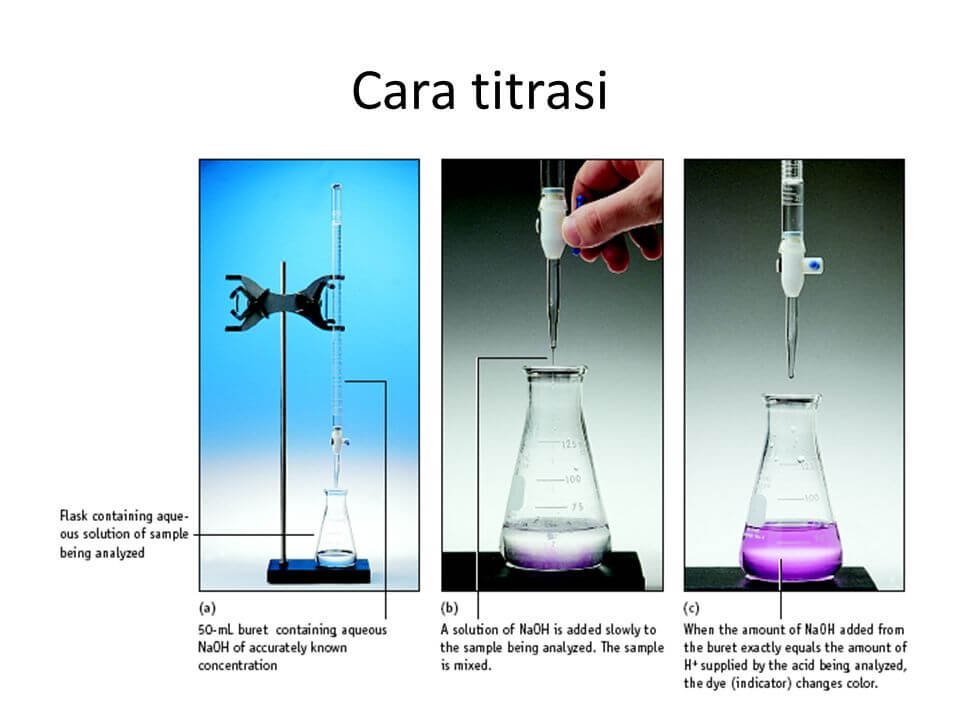
Soal Dan Jawaban Titrasi Asam Basa My XXX Hot Girl
Titrasi adalah teknik analitik yang memungkinkan penentuan kuantitatif zat spesifik yang terlarut dalam sampel.. (titrasi, titer, titran, indikasi, analit, dll.) Unduh buku pedoman untuk mempelajari semuanya tentang dasar-dasar titrasi. Dalam buku pedoman ini, Anda akan menemukan informasi dasar yang bermanfaat tentang berbagai teknik yang.

Berdasarkan grafik tersebut, larutan yang berperan sebaga...
Jawabannya. HCl + NH 3 NH 4 Cl , maka valensi = 1. M a x V a = M b x V b. 0.105M x V a = 0.118M x 22.5mL. V a = 25.3 mL. Itulah tadi beberapa materi yang dapat dituliskan terkait dengan pengertian titrasi asam basa, cara kerja, macam, rumus perhitungan, contoh soal dan jawabannya. Semoga melalui ulasan ini bisa memberikan wawasan serta menambah.

Titrasi Argentometri metode Mohr (Tutorial Prosedur analisis kadar NaCl
Adapun titran ialah larutan standar yang telah diketahui konsentrasinya. Sementara indikator asam basa adalah zat yang bisa mengalami perubahan warna saat mendekati titik ekivalen. Contoh larutan yang dapat dicari kadarnya (konsentrasinya) dalam titrasi, salah satunya larutan asam berupa asam klorida (HCl).

tentukan volume masing masing titran yang diperlukan dalam titrasi
Highly automated potentiometric & Karl Fischer titrators. FDA certified, Get a quote now! In Stock, Best price, Global maintenance service, OEM Service Available, Get quotes now

Different Methods of Measuring Drug Potency, Concentration, Efficacy
Sedangkan, zat peniter (titrat) adalah larutan baku yang sudah diketahui jumlah konsentrasinya dan dimasukan ke dalam buret. Prinsip Titrasi Asam Basa Titrasi asam basa melibatkan dua jenis larutan, yaitu larutan basa dan larutan asam yang dapat menempati dua peran sebagai zat dititrasi (titran) dan zat peniter (titrat).

Istilah Titrasi Asam Basa Ilmu Kimia
Definisi Titran dalam Kimia. Corbis melalui Getty Images / Getty Images. Diperbarui pada 30 November 2018. Dalam kimia analitik, titran adalah larutan yang konsentrasinya diketahui yang ditambahkan ( dititrasi ) ke larutan lain untuk menentukan konsentrasi spesies kimia kedua. Titran juga dapat disebut titrator , reagen , atau larutan standar .
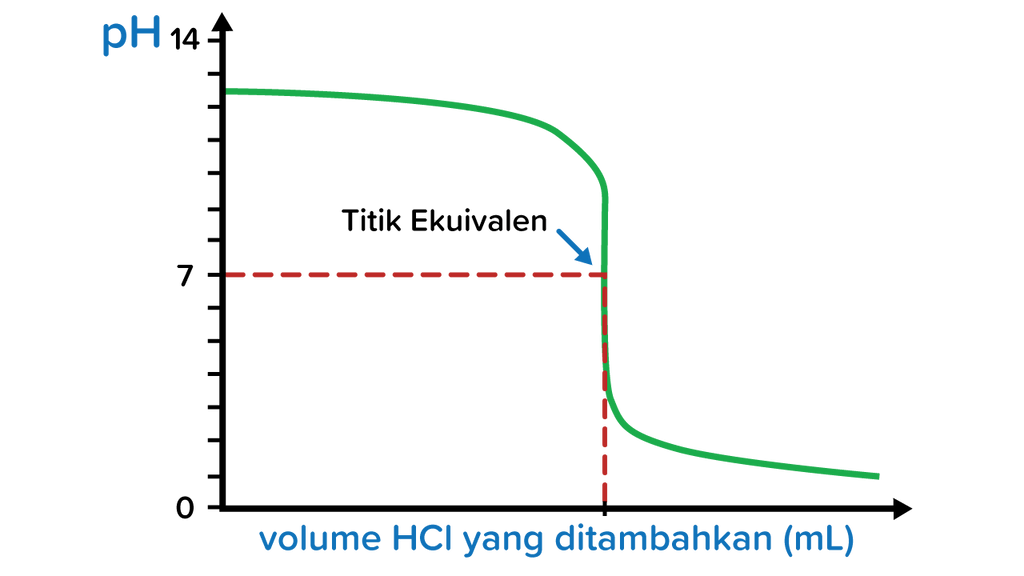
Tentukan konsentrasi titran dan buatlah grafik tit...
Indikator ini ditambahkan pada titran sebelum melakukan proses titrasi. Penambahan indikator diusahakan sesedikit mungkin dan umumnya adalah 2 ‒ 3 tetes menggunakan pipet. Perubahan warna saat titran yang telah ditambahkan indikator menjadi tanda bahwa proses yang berlangsung telah mencapai titik ekivalen.